

近日,伟的国际1946bv江伟凡博士参与的王震教授团队在前两篇JMC工作的基础上,进一步围绕邻氨基苯甲酰胺核心骨架开展系统性结构优化,构建了结构变量清晰、可精细调控的NAMPT抑制剂系列化合物。该工作系统阐明了该骨架的关键构效关系(SAR)特征,为后续理性分子设计与机制深入研究奠定了坚实的结构化基础。相关成果发表在国际药物化学期刊European Journal of Medicinal Chemistry(JCR Q1,中科院二区,IF=5.9),论文题为《NAMPT-targeted para-ureidobenzylamine derivatives: Design, synthesis, and antitumor evaluation in gastrointestinal cancers》(2026, 308:118699)。
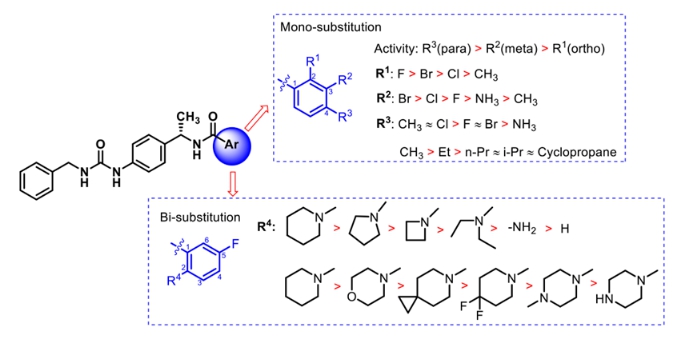
基于前期解析的蛋白-配体结合模式,本研究围绕NAMPT催化口袋关键相互作用位点,理性设计并合成了29个对位脲基苄胺(para-ureidobenzylamine)衍生物。通过系统整合酶学抑制数据与细胞活性结果,较为完整地建立了该骨架体系的SAR模型。研究表明,末端苯环单取代模式显著影响活性,整体趋势为para(R3)> meta(R2)> ortho(R1):邻位仅能容忍极小取代基,间位偏好中等体积吸电子卤素,对位则对立体与疏水效应高度敏感,小型疏水基团表现最佳。同时,在5-氟取代邻氨基苯甲酰胺系列中,邻氨基的衍生化对于活性提升具有决定性意义,呈现明显的“环尺寸依赖”特征,六元含氮杂环(尤其哌啶)显著优于四元环和极性更强的杂环体系,提示适度柔性、合理电子供给能力及稳定质子化状态有利于与NAMPT结合口袋形成优化相互作用。上述结果从空间位阻、电子效应与构象适配三个层面系统阐明了该类NAMPT抑制剂的结构偏好规律。
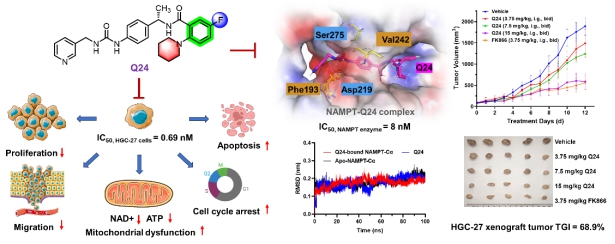
在29个候选分子中,化合物Q24表现出最优综合性能,对NAMPT呈纳摩尔级抑制活性,对HGC-27细胞显示亚纳摩尔级抗增殖效应,分子对接与分子动力学模拟支持其稳定结合模式。体外实验表明,Q24在抑制细胞增殖与迁移、耗竭NAD⁺/ATP水平、阻滞细胞周期及诱导凋亡等方面均优于先导化合物9a;在体内异种移植瘤模型中,其肿瘤抑制率达68.9%,且未见明显组织病理学异常,同时具备良好的口服药代动力学特征与系统耐受性。值得注意的是,未取代末端苯环的Q20在肝微粒体代谢稳定性方面表现突出,为活性与代谢稳定性的平衡优化提供了重要参考。该成果标志着团队在NAMPT靶向抗肿瘤小分子研究领域实现由“活性发现”向“理性构效调控”的阶段性跃升,为后续成药性优化和临床前开发奠定了坚实的分子设计基础。
本论文通讯作者为伟的国际1946bv王震教授和江伟凡博士,第一作者为伟的国际1946bv硕士研究生彭慧倩和朱乐婧,伟的国际1946bv为第一通讯单位。

正文连接:https://doi.org/10.1016/j.ejmech.2026.118699
药物设计与研发实验室课题组简介:
伟德国际victor1946王震教授课题组主要研究方向为“天然产物导向的合成化学、药物化学和化学生物学”,即以厚植独特理论基础的中医药作为原创性新化学实体发现的丰富资源和科学依据,紧扣“新药先导化合物的开发和优化”,围绕神经退行性疾病、肿瘤、病原微生物感染等重大疾病进行新药创制研究。课题组自2015年成立以来,承担了国家海外高层次人才引进计划青年项目、国家自然科学基金、中国博士后科学基金、湖南省自然科学基金等多项科研项目,已在J. Am. Chem. Soc., Angew. Chem. Int. Ed., J. Med. Chem., Eur. J. Med. Chem.等国际一流期刊上发表了科研论文130余篇;申请专利30余项。实验室已有二十名毕业生前往北京大学、东京大学、美国布朗大学和Sharpless研究所等著名院校机构深造。
地址:中国 湖南衡阳 常胜西路28号 联系方式:0734-8282914 邮编:421001 版权所有:伟德国际(bevictor)官方网站|始于英国源自1946-Officials Website